循環式養殖(アクアリウム含む)の
「水質管理」シリーズ⑤
循環式養殖についての記事はこちら(循環式養殖の水質管理)
目次
「アンモニア」と「亜硝酸」の毒性について
なぜ「アンモニア」と「亜硝酸塩」の特性について知る必要があるのか?
循環式養殖では水槽内で毒性の高い「アンモニア」や「亜硝酸塩」が発生します。
そのため、それらの有害な物質は生物ろ過によって処理して無害化しています。
窒素循環について記事はこちら↓
 【水質管理】窒素循環とは?(アンモニア→亜硝酸→硝酸)どのように分解されるのか?
【水質管理】窒素循環とは?(アンモニア→亜硝酸→硝酸)どのように分解されるのか?
水槽内の「アンモニア」や「亜硝酸塩」はできるだけ、
低い状態で管理することが「理想的」です。
アクアリウムのように鑑賞用で飼育する場合は、
濾過槽を自由に設置できますが、養殖では制限があります。
養殖で濾過槽が大きくなると言うことはコストが上がるため、
「生産原価のアップ」に直結します。
具体的には濾過槽が大きくなると「濾過槽の面積」や「ろ材の量」も
増えてイニシャルコストが上がります。
また、濾過槽の水量が増えることで、水槽全体の水量が大きくなり
「加温費」等のランニングコストもあがります。
そのため、養殖場の濾過槽の設計は「オーバースペック」ではなく
「適正なサイズ」で運用しなければなりません。
さらに、実際の養殖場で育成管理をしていく際には生産量を高めるため、
できるだけ飼育している生き物に影響のでない範囲でギリギリの水質を攻めます。
このギリギリを攻めるためにも「アンモニア」や「亜硝酸」が高いと
「どのような影響がでるのか?」
「どのような条件下で毒性が高くなるのか?」
といった特性をきちんと理解する必要があります。
今回の記事では「アンモニア」と「亜硝酸塩」の
毒性と特性についてわかりやすく説明していきます。
アンモニアの毒性について
アンモニアはどのように「発生」するのか?
餌の中のタンパク質などの窒素化合物は水生生物の体内で分解されて、
アミノ酸単位まで分解されて利用されます。
しかし、その中で成長に使われる窒素源は約30%であり、
残りの約70%は「窒素性排出物」として排出されます。
この「窒素性排出物」の中の50%は「アンモニア」として育成中に放出されます。
(魚介類はフンとしてだけでなく、エラからも直接育成水中にアンモニアを放出します。)
アンモニアの「測定方法」
育成水中のアンモニア濃度は「アンモニア態窒素」の量を
測定すること調べることができます。
アンモニア態窒素量は水中のすべてのアンモニアの窒素分の量を測定します。
これは簡易的は水質検査キットでも調べることができます。
水質の測定方法についての詳しい記事はこちら↓
 【簡単計測】アンモニア値の測定方法~水槽の水質測定おすすめキット~
【簡単計測】アンモニア値の測定方法~水槽の水質測定おすすめキット~
アンモニアの「種類」と「毒性」について
飼育水の中で放出されたアンモニアは
毒性の異なる2種類のアンモニアとして存在します。
①難脂溶性のアンモニウムイオン(NH4+)
②脂溶性のアンモニア(NH3)
この2つのアンモニアの窒素の濃度を合計した値が
「アンモニア態窒素」です。
難脂溶性のアンモニウムイオン(NH4+)は毒性が低いのですが、
脂溶性のアンモニア(NH3)は細胞膜を簡単に通過します。
そのため、細胞機能に直接影響を与えるため毒性が非常に高いです。
アンモニア(NH3 )の毒性は、アンモニウムイオン(NH4+)の毒性の300倍~400倍とも言われています。
魚種等によってアンモニアの耐性はことなりますが、アンモニアNH3が0.05mg/L以下で保つのが理想的です。
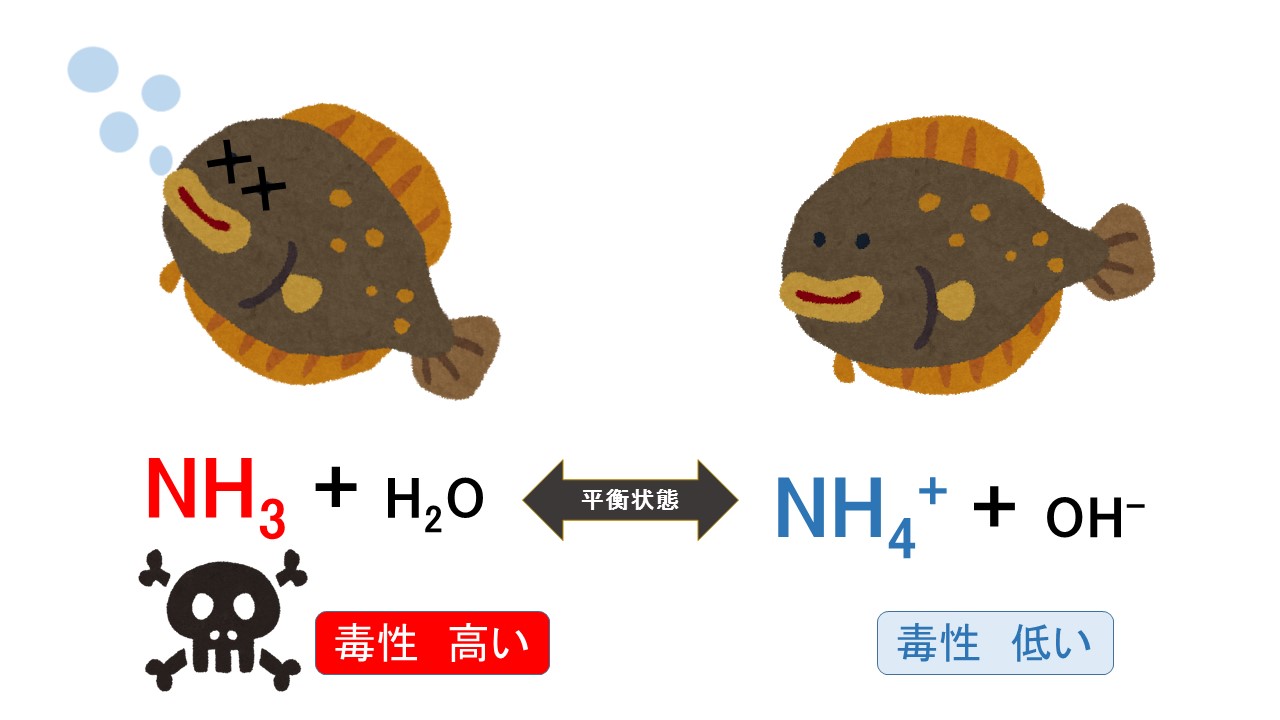
この2種類のアンモニアは水中では下記の化学式のような形で平衡状態を保っています。
※「平衡状態」とは
順方向の反応と逆方向との反応速度が釣り合って反応物と生成物の組成比が巨視的に変化しないこと。
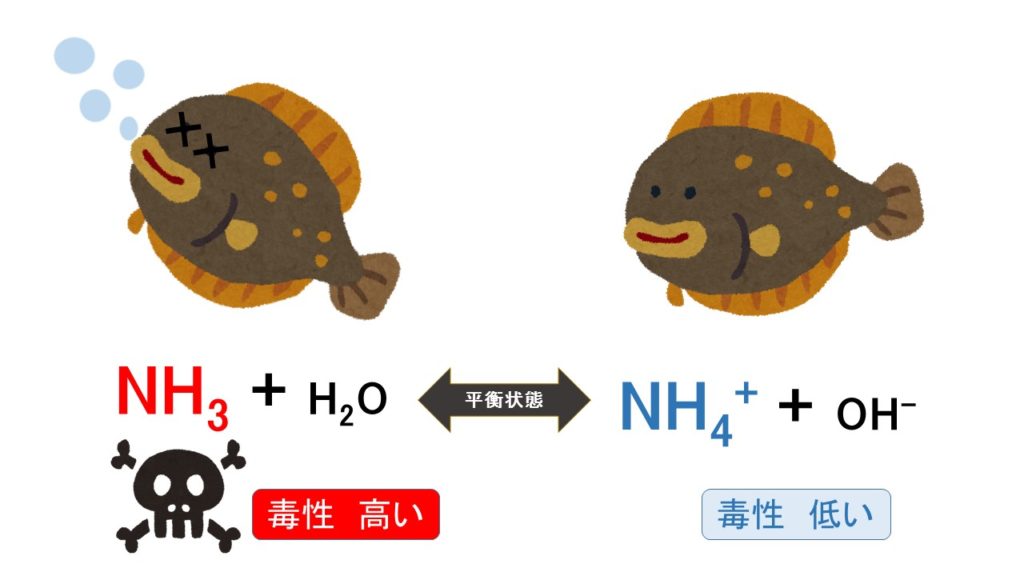
(↑化学式:アンモニア(NH3)とアンモニウムイオン(NH4+)の関係)
しかし、水中でのアンモニアとアンモニウムイオンの割合は常に一定ではありません。
アンモニアとアンモニウムイオンの割合は飼育水の条件によって変化します。
特に「pH」や「水温」が変化するとこの割合は大きく変わってきます。
下記の図は塩分濃度が28~33g/L(海水条件下)の脂溶性のアンモニア(NH3)の割合です。
| 海水条件 | 水温 | ||
| pH | 20℃ | 25℃ | 30℃ |
| 5.5 | 0.01 | 0.01 | 0.02 |
| 6.0 | 0.03 | 0.05 | 0.07 |
| 6.5 | 0.1 | 0.15 | 0.21 |
| 7.0 | 0.32 | 0.47 | 0.67 |
| 7.5 | 1.01 | 1.46 | 2.10 |
| 7.7 | 1.59 | 2.29 | 3.29 |
| 8.0 | 3.12 | 4.47 | 6.36 |
| 8.2 | 4.86 | 6.9 | 9.72 |
(↑図:脂溶性のアンモニア(NH3)の割合)
参考:循環式陸上養殖よりデータ引用
アンモニアの「管理方法」
実際に水槽内の水質を管理する場合は、
まず「アンモニア態窒素」を測定します。
そのうえで飼育水の「pH」と「水温」を上記の表で確認し、
「脂溶性のアンモニア(NH3)」の量を計算します。
アンモニア態窒素(すべてのアンモニアの量)×脂溶性割合=脂溶性のアンモニア量
例えば、水槽の条件がpH8で水温25℃、アンモニア態窒素が1mg/Lの場合の脂溶性アンモニアの量は
1mg/L×4.47%=0.047mg/Lとなります。これであれば基準値の0.05mg/L以下となります。
亜硝酸の毒性について
「亜硝酸」は循環式の水槽の中で発生します。
発生原因はアンモニアが硝化細菌によって分解されると亜硝酸になるためです。
亜硝酸硝化細菌の方がアンモニアの硝化細菌よりも能力が高いため、
通常は亜硝酸よりも先にアンモニアの方が問題になる場合が多いです。
しかし、亜硝酸硝化細菌はアンモニア硝化細菌より
フル稼働するまでに時間がかかるります。
そのため、育成を開始したばかりの水槽ではアンモニアだけが分解され、
亜硝酸ばかりが溜まってしまうといった問題が発生するので注意が必要です。
亜硝酸の「測定方法」
亜硝酸もアンモニアと同様に「簡易水質検査キット」
で測定することができます。
水質の測定方法についての詳しい記事はこちら↓
 【簡単計測】アンモニア値の測定方法~水槽の水質測定おすすめキット~
【簡単計測】アンモニア値の測定方法~水槽の水質測定おすすめキット~
亜硝酸の「毒性のメカニズム」
アンモニアが水生生物の細胞に直接影響を与えるのに対して、
亜硝酸は酸素を運搬する機能を奪い酸欠による斃死を引き起こします。
亜硝酸イオン(NO2–)は酸素を運搬する機能を持つヘモグロビンを
メトヘモグロビンという成分に変えてしまいます。
そのため、水生生物の体内に酸素が不足して死んでしまうのです。
これが「亜硝酸中毒」です。
また、亜硝酸イオン(NO2–)はエラから血中に入っていきます。
さらに、エラから取り込まれる亜硝酸イオン(NO2–)は塩化物イオン(Cl–)と競合して
エラから取り込まれることも分かっています。
そのため、塩化物イオン(Cl–)の多い飼育環境では亜硝酸イオン(NO2–)
が取り込まれにくくなるため亜硝酸の毒性が低くなります。
(↑図:亜硝酸イオンと塩化物イオンの競合イメージ)
~参考~
塩化物イオン(Cl–)は塩分の量を表す指標で、
「塩分濃度」が高いと塩化物イオン(Cl–)も多くなります。
つまり、亜硝酸の毒性は塩化物イオンの多い「海水」では毒性が低くなり、
「淡水」では非常に高くなります。
そのため、淡水での亜硝酸管理には注意が必要です。
参考文献:
・循環式陸上養殖
・養殖の餌と水
 循環実装ラボ
循環実装ラボ